Come determinare il punto isoelettrico?
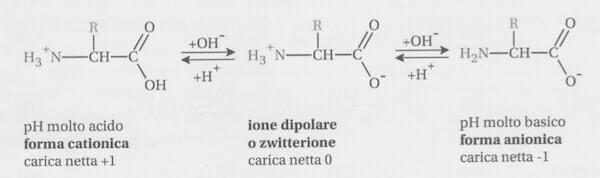
Il punto isoelettrico, o pH isolettrico, è un valore che viene stabilito in biochimica, ovvero in quel ramo della scienza che si occupa dello studio della biologia e della chimica in relazione allo studio degli organismi viventi, fra cui l’uomo. Fra le macromolecole più importanti negli esseri viventi ci sono le proteine, che producono enzimi che sono in grado di innescare diverse funzioni nell’organismo. Le proteine sono costituite da strutture complesse, ognuna delle quali è formata da una serie di amminoacidi. Questi sono legati fra loro da legami chimici di tipo peptidico (dal termine peptidi, sinonimo di amminoacidi).

Per calcolare il punto isoelettrico, bisogna fare la media del PK2 (l’amminico) e del PKr. Questo perché il pH è compreso fra il PK1 ed il PK2, e il residuo è basico. Prendendo come esempio l’istidina, questo amminoacido ha un PK2 = 9,18 ed il PKr = 6,10. Sostituendo i valori, si ottiene PI = (9,18 + 6,10) / 2 = 7,64.
Cosa influenza il punto isoelettrico?
Il valore del punto isoelettrico è molto importante per le operazioni di separazione e purificazione delle proteine perché corrisponde alla condizione in cui la solubilità è minima e la mobilità, in un campo elettrico, è zero (quindi la proteina si accumula).
Quali molecole si usano per determinare il punto isoelettrico?
Punto isoelettrico degli amminoacidi
- pH = 5,97 per la glicina;
- pH = 6,01 per la alanina;
- pH = 5,96 per la valina;
- pH = 5,98 per la leucina;
- pH = 6,02 per la isoleucina;
- pH = 5,48 per la fenilalanina;
- pH = 5,74 per la metionina;
- pH = 6,30 per la prolina;
Come si forma lo zwitterione?
Un zwitterione è una molecola neutra che presenta sia gruppi acidi che basici nella sua struttura. Questi gruppi sono presenti in quantità uguali, il che significa che la molecola non ha una carica netta. Tuttavia, questa molecola può comportarsi come un acido o una base a seconda del pH dell’ambiente circostante.
Questa proprietà di ionizzazione dipende dal fatto che gli atomi che compongono il gruppo acido o basico hanno differenti elettronegatività, creando una distribuzione asimmetrica delle cariche parziali nella molecola. I composti che si presentano come zwitterioni sono generalmente poco solubili nei solventi organici a causa della loro natura ionica, mentre sono abbastanza solubili in acqua a causa della sua capacità di formare legami ionici con gli ioni positivi e negativi della molecola.
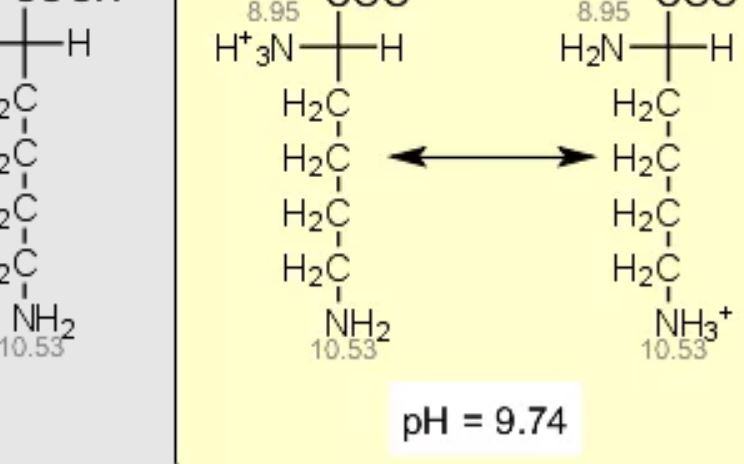
Qual è la carica della lisina a pH 11?
Un amminoacido basico: la lisina
Nel punto isoelettrico la carica netta della maggior parte degli amminoacidi presenti in soluzione è zero.
Determinazione del punto isoelettrico della glicina (parte 1)
https://www.youtube.com/watch?v=Q5ye-z7R_eQ
Il punto isoelettrico, o pH isolettrico, è un valore che viene stabilito in biochimica, ovvero in quel ramo della scienza che si occupa …
Per tutti gli aminoacidi senza residuo ionizzabile, il punto isoelettrico si calcola con la semplice media tra il pK carbossilico (pK1) ed …
Come calcolare il punto isoelettrico
Come calcolare il punto isoelettrico dei peptidi
Dove viene prodotta la tirosina?
Non si tratta di un aminoacido essenziale in età adulta perché può essere sintetizzato dall’organismo a partire da un altro aminoacido, la fenilalanina. È presente nei latticini, nella carne, nel pesce, nelle uova, nella frutta secca, nei legumi, nell’avena e nel grano.
Quali sono i 20 amminoacidi?
Strutture molecolari standard dei 20 amminoacidi proteinogenici.
- Alanina. (Ala / A)
- Arginina. (Arg / R)
- Asparagina. (Asn / N)
- Acido aspartico. (Asp / D)
- Cisteina. (Cys / C)
- Acido glutammico. (Glu / E)
- Glutammina. (Gln / Q)
- Glicina. (Gly / G)
Come sono classificati gli aminoacidi?
Struttura generica degli amminoacidi
Ogni amminoacido presenta uno specifico gruppo laterale (detto anche gruppo R). In funzione delle proprietà chimiche di tale gruppo, un amminoacido viene classificato come acido, basico, idrofilo (o polare) e idrofobo (o apolare).
Che cosa si intende per aminoacido in forma di ione dipolare?
A destra la struttura dipolare di un amminoacido (zwitterione). Lo ione dipolare (zwitterione) è la specie predominante a un pH corrispondente al punto isoelettrico. Lo ione dipolare viene chiamato anche sale interno o struttura (0). Nonostante tale struttura ionica, la solubilità in acqua dello zwitterione è modesta.
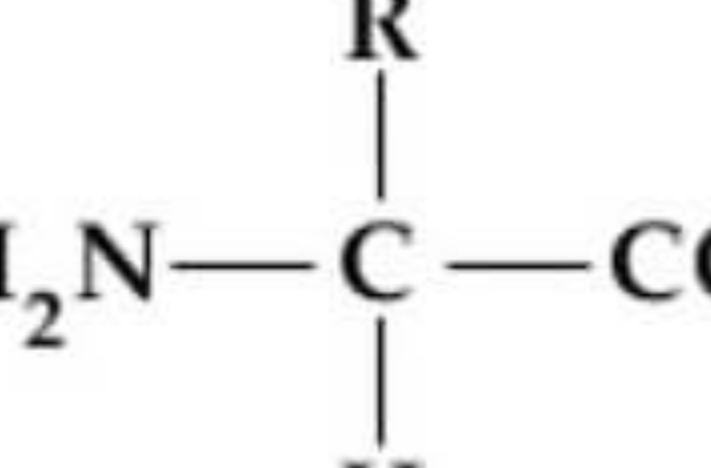
Come è fatto un amminoacido?
La struttura di un alfa-amminoacido è riportata in figura 1. All’atomo di carbonio alfa sono legati un gruppo carbossilico (-COOH), un gruppo amminico (-NH2), un atomo di idrogeno ed una catena laterale (gruppo R). … L’atomo di carbonio alfa è detto asimmetrico o chirale perché lega quattro gruppi diversi.
A cosa serve il pKa?
pKa è il log negativo della costante di dissociazione acida o valore Ka. Un valore pKa inferiore indica un acido più forte. Cioè, il valore più basso indica che l’acido si dissocia più completamente in acqua.
Quanti sono gli aminoacidi essenziali?
Nell’essere umano adulto quelli essenziali sono 8: fenilalanina, treonina, triptofano, metionina, lisina, leucina, isoleucina e valina – questi ultimi 3 hanno anche le proprietà di amminoacidi ramificati (BCAA). per i soggetti in accrescimento è compresa anche l’istidina.
Che cosa sono gli aminoacidi essenziali?
La nostra salute dipende da un’adeguata disponibilità di 9 aminoacidi essenziali. Fra questi, i più conosciuti sono i cosiddetti ramificati (BCAA) Leucina, Isoleucina e Valina mentre i restanti 6 sono Metionina, Treonina, Lisina, Fenilalanina, Istidina e Triptofano.
Come rompere un legame peptidico?
L’idrolisi enzimatica è la reazione più semplice per rompere un legame covalente peptidico. Essa consiste nella reazione inversa alla condensazione: con l’aggiunta di acqua e l’azione di un enzima si passa dai prodotti ai reagenti, quindi, nel caso di un dipeptide, ai due amminoacidi separati.
Cosa si ha in un peptide formato da 5 amminoacidi?
le encefaline (5 aminoacidi), con funzioni di neurotrasmettitori. la bradichinina (9 aminoacidi), altro neurotrasmettitore. l’ossitocina (9 aminoacidi), che biologicamente svolge la funzione di ormone. il peptide intestinale vasoattivo (VIP, 28 aminoacidi), ormone attivo nell’intestino e in altri organi.
Come si scrive un peptide?
Un peptide viene denominato iniziando con il nome dell’aminoacido che ha il gruppo amminico libero, sostituendo con il suffisso “il” la desinenza “ina”. Si continua poi con tale sostituzione per tutti gli amminoacidi della catena, fino all’ultimo aminoacido, che mantiene invece il nome normale.
Che cosa sono i peptidi?
I peptidi sono sostanze di sintesi, formate da due o più amminoacidi. Quando gli amminoacidi si uniscono in una certa formazione creano specifici peptidi, e quando questi ultimi si uniscono a loro volta, creano specifiche proteine. I peptidi dunque, possono essere definiti frammenti di proteine.
Quale tra queste è una caratteristica degli amminoacidi?
Una caratteristica peculiare degli amminoacidi è quella di agire sia come basi che come acidi. Quando un AA è sciolto in H2O diventa uno ione dipolare o zwitterione. Uno zwitterione può agire sia come acido, quindi essere un donatore di protoni che come base, quindi essere un accettore di protoni.
Perché gli amminoacidi hanno comportamento Anfotero?
Gli amminoacidi hanno comportamento anfotero, poiché possono reagire sia come acidi, donando un protone, sia come basi, accettando un protone: … D’altra parte, in ambiente basico l’amminoacido si trova sotto forma di ione negativo, che migra verso l’anodo.
Dove si trovano in natura gli aminoacidi?
Leucina: latte, mais, pollo e uova sono le fonti principali di questo aminoacido che, a differenza degli altri AEE, si trova anche nei cereali e nei legumi che di solito ne sono poveri. Si può trovare anche in ricotta, sesamo, arachidi, lenticchie e pesce.
Cosa vuol dire Alfa amminoacidi?
Qual è la funzione degli aminoacidi?
Gli aminoacidi sono molecole organiche che svolgono una serie di funzioni collegate al metabolismo cellulare ma, ancora più importante, rappresentano i componenti fondamentali delle proteine e sono necessari per una normale crescita e per lo sviluppo del corpo umano.
Cosa sono gli amminoacidi biologia?
Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di “mattoni” di amminoacidi. … Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di “mattoni” di amminoacidi.
Come si prendono gli aminoacidi essenziali?
Dovrai fare in modo di assumere alimenti ricchi di proteine, quali legumi, noci, prodotti caseari, pesce e carne. Dovrai anche prestare attenzione alla qualità delle proteine negli alimenti. Gli integratori, quali le proteine in polvere e le barrette proteiche, rappresentano un’altra possibile fonte di aminoacidi.
Perché aminoacidi essenziali?
Gli aminoacidi essenziali hanno dimostrato azioni benefiche su un ampio spettro di tessuti e sistemi, migliorando: Funzioni immunitarie. Omeostasi del glucosio e sensibilità all’insulina. Funzioni cardiaca e renale nei pazienti diabetici.
Perché 8 amminoacidi sono definiti essenziali?
Dei 23 aminoacidi indispensabili al nostro organismo, 8 sono definiti essenziali (AAE), ovvero non sintetizzabili. Questo significa che, essendo necessari ma non sintetizzabili, vanno introdotti con l’alimentazione. Questi 8 sono: Lisina, Leucina, Isoleucina, Metionina, Triptofano, Fenilalanina, Valina, Treonina.
I peptidi sono brevi frammenti polimerici composti da aminoacidi. Ogni peptide ha una certa sequenza di amminoacidi denotata con un codice di tre lettere o …
Il punto isoelettrico (pI) è il valore di pH al quale una molecola presenta carica elettrica netta nulla. Per un amminoacido avente un solo gruppo amminico …
Il punto isoelettrico (pl) è il pH (indice di acidità della soluzione) a cui una molecola in soluzione ha una carica netta pari a zero.
Punto isoelettrico
Punto isoelettrico, il valore di pH: cos’è e come si calcola
Zwitterione. La carica netta presente in una molecola anfolitica, come quella di un amminoacido, è influenzata dal pH: si definisce punto isoelettrico il valore …
Stai guardando: Come determinare il punto isoelettrico?
Fonte: townhouserome
Categoria: Qual è lo